MEDCH – Wo Arzneimittelinformation zu Wissen wird
Neue Wege in der Pharmakommunikation erfordern Mut – und die Bereitschaft, echten Wissenstransfer in den Mittelpunkt zu stellen. Genau hier setzt MEDCH an.
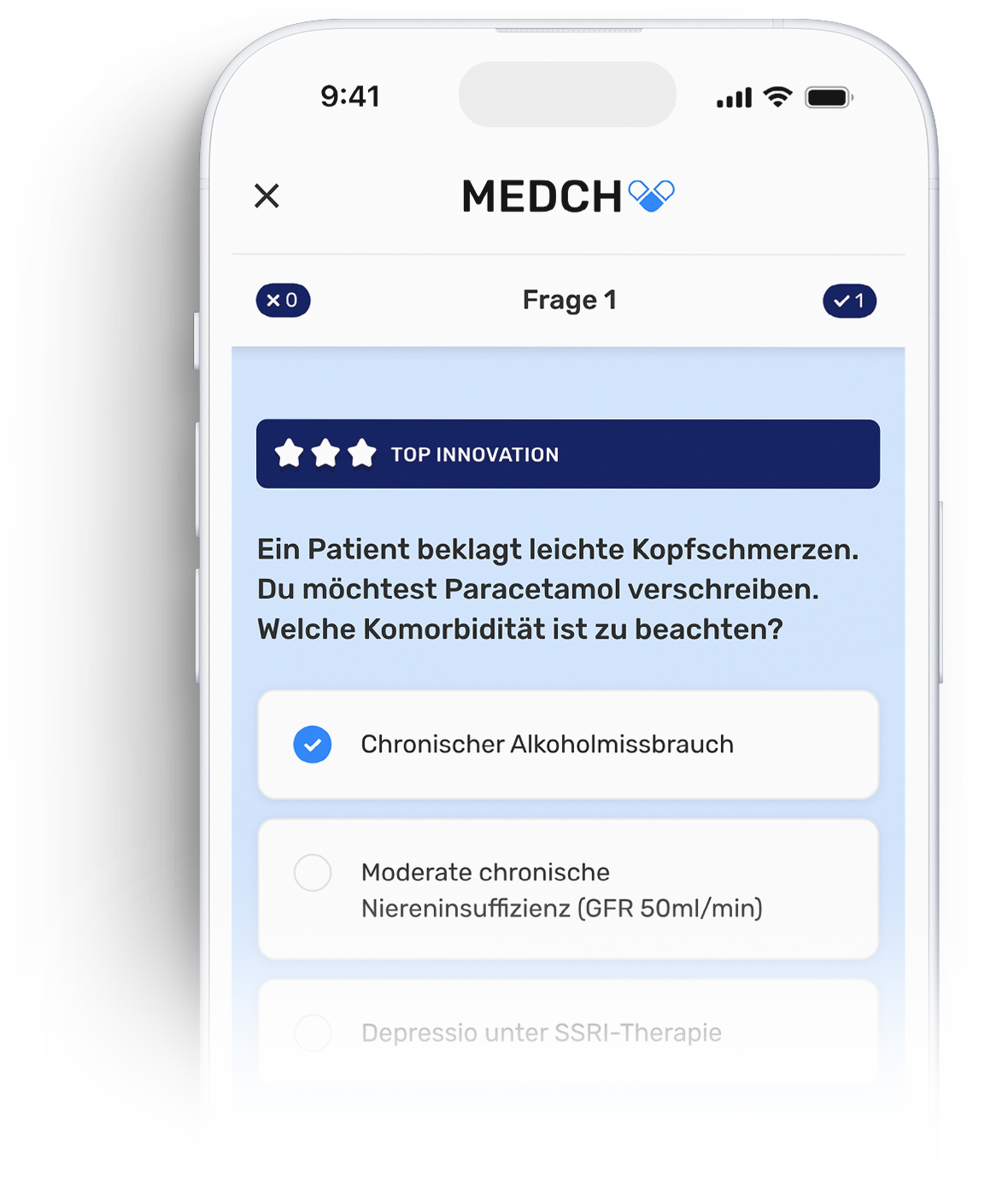
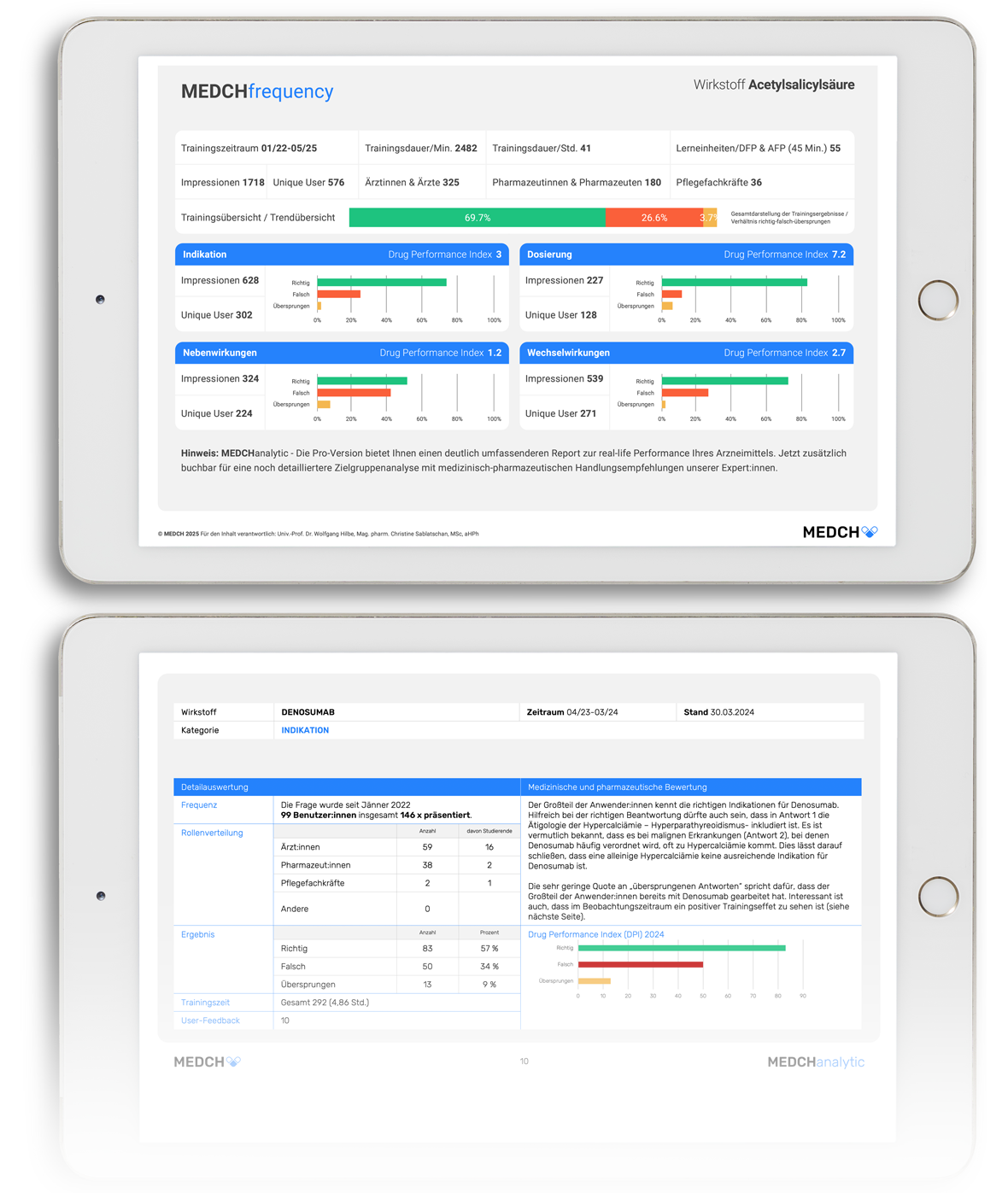
MEDCH ist ein digitales Lern- und Trainingssystem für medizinisches Fachpersonal – entwickelt, um Medikationssicherheit im klinischen Alltag gezielt zu stärken. In interaktiven, realitätsnahen Fallbeispielen trainieren Ärzt:innen, Pharmazeut:innen und Pflegekräfte konkrete Entscheidungssituationen: indikationsgerecht, praxisnah, evidenzbasiert.
So entsteht nachhaltiges Wissen, das die sichere Anwendung von Arzneimitteln fördert – und letztlich der Patientensicherheit dient.